Después de hablar de los átomos, la tabla periódica, las moléculas, los gases y el agua, ahora toca revelar cómo se unen los átomos para crear todo lo que existe. A través de los enlaces químicos, los elementos dejan de estar aislados y comienzan a cooperar: comparten, transfieren y forman estructuras estables.
Desde la química, esto se manifiesta en enlaces iónicos, covalentes, metálicos, etc. Desde un aspecto más simbólico, podemos reflexionar sobre el arte de vincularse sin perder la identidad, y cómo la unión trae nuevas propiedades emergentes.
Hasta ahora vimos que todo está hecho de átomos. Pero los átomos por sí solos no construyen ni células, ni montañas, ni recuerdos. La complejidad aparece cuando los átomos se unen sin perder su identidad, pero generando algo nuevo.
Aunque los científicos no han llegado a un acuerdo de cómo definir un enlace rigurosamente, en términos simples, un enlace químico es una fuerza que mantiene unidos a los átomos. Pero algo que debemos destacar, es que en el enlace químico se llega a un acuerdo energético, donde los electrones se reorganizan para que todos los átomos involucrados ganen estabilidad.
En esta entrega nos vamos a centrar en los tres tipos de enlace más comunes (aunque no los únicos):
Enlace iónico. Aquí, un átomo cede electrones y otro los recibe. Se dice que se atraen por diferentes electronegatividades. Simbólicamente puede representar vínculos por necesidad o compensación. Un ejemplo de este tipo de enlace es el NaCl que conocemos como cloruro de sodio o sal de mesa.
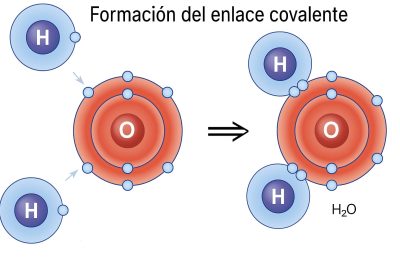
Enlace covalente. En este enlace los átomos comparten electrones. Podemos decir que los átomos colaboran entre ellos. En una analogía humana, podemos hablar de vínculos equilibrados o consientes. Dos ejemplos de este tipo de enlace son el agua (H₂O) y el oxígeno (O₂), dos moléculas de las que ya hablamos en entregas anteriores.
Enlace metálico. Este tipo de enlace es peculiar ya que los electrones fluyen como un mar colectivo entre todos los átomos. Esto los convierte en buenos conductores de electricidad, por ejemplo, los cables de cobre metálico. Simbólicamente, esta unión podría representar la comunidad, la pertenencia y la cooperación fluida. Ejemplos de este enlace es el que ocurre en el oro y el cobre que ya mencioné.
Una vez que los átomos se unen, el resultado es más que la suma de sus partes. Por ejemplo, el cloro por sí solo es tóxico y el sodio es muy reactivo, pero unidos forman el NaCl, vital para la vida ya que es indispensable en procesos biológicos celulares. Es decir, su unión tiene una función en la evolución humana.
Si trasladamos esto a la vida, sabemos que las relaciones auténticas nos cambian. Nos dan nuevas cualidades y nos vuelven más humanos.
La próxima vez que pensemos en una molécula debemos reconocerla como una red de cooperación. Como átomos que dejaron existir solos para formar algo más grande, y funcional que vibra y evoluciona.
Por último, y recordando que podemos reconocernos a nosotros mismos como átomos macroscópicos con cualidades únicas:
– ¿Qué tipo de enlaces construyo en mi vida?
– ¿Cómo cambia mi energía cuando me vinculo?
– ¿Con quién formo estructuras estables?
Excelente fin de semana, nos vemos en la próxima entrega.
Mariano Sánchez Castellanos Postdoctor en Astrofísica Molecular.
“Un encuentro entre la Espiritualidad y la Ciencia”
